Boyle's Gesetz
Wenn man das Volumen eines Gases verkleinert (z.B. durch einen Kolben zusammenpresst), so erhöht sich der Druck in gleichem Maße, wenn die Temperatur dabei konstant bleibt. Halbiert man das Volumen, so verdoppelt sich der Druck.
auch bekannt als:
Wenn man Vakuum erzeugt, also den Druck sehr stark erniedrigt, dann expandieren Gase zu enormen Volumen (entsprechend Boyle's Gesetz). Dies geschieht auch mit absorbiertem Gas, z.B. aus Fingerabdrücken oder Schmutz.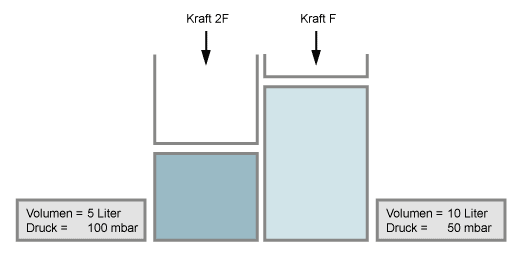
bei gleicher Anzahl von Molekülen (Temperatur konstant gehalten)


